酸化還元反応とは?反応式の書き方・コツをわかりやすく解説|高校生向け受験応援メディア「受験のミカタ」
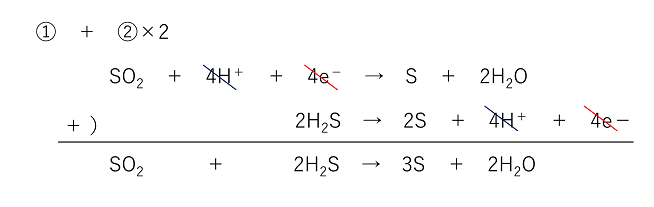
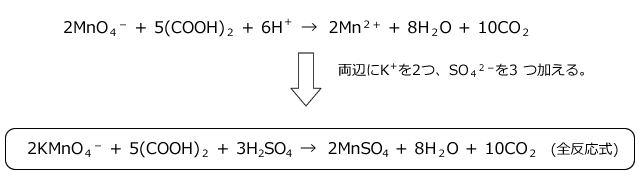
この反応式を全反応式と言います。 つまりMn原子にだけ注目すれば、 電子7個が不足する状態から 電子2個が不足する状態へ変化した、 ということになります。 この問題の場合、求めたいのは濃度不明の還元剤の濃度 c' であり、方程式で移項して計算すれば求まる。
15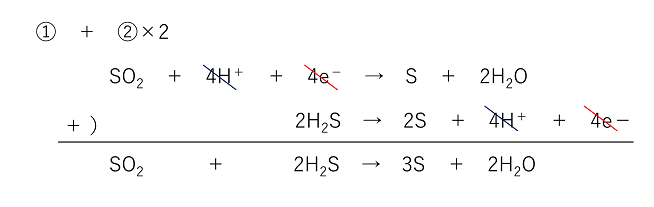
この反応式を全反応式と言います。 つまりMn原子にだけ注目すれば、 電子7個が不足する状態から 電子2個が不足する状態へ変化した、 ということになります。 この問題の場合、求めたいのは濃度不明の還元剤の濃度 c' であり、方程式で移項して計算すれば求まる。
15具体例 [ ]• 例えば、金属のは中の酸素分子と徐々に反応し、表面は褐色の CuO に変化する。
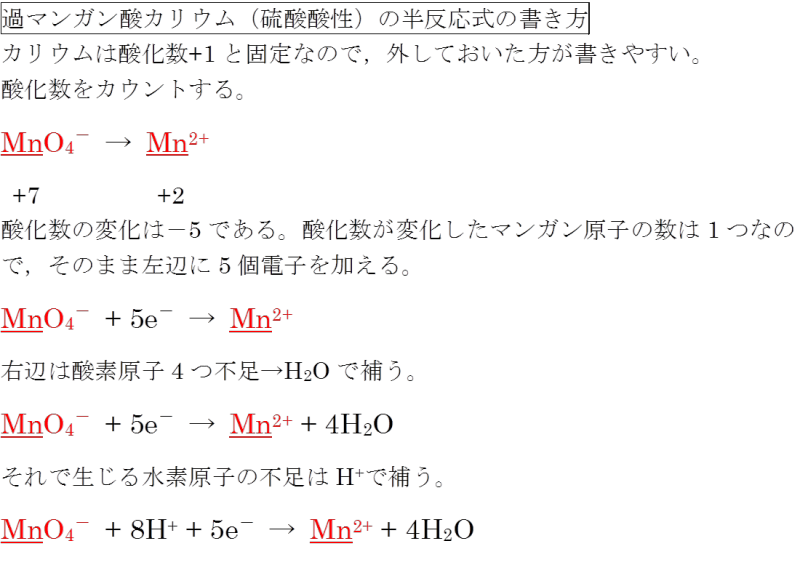
4.酸化還元反応の必須知識:酸化数って?? 上記で説明した通り、 酸化数とは、電子の形式的な電荷がどう変化しているか知るための値のことを言います。
5また電子反応論に立つと、前者の銅の酸化反応では、銅は電子を2個失い、同時に酸素(原子)は銅からその2個の電子を受け取ってを満たす酸化物イオンとして安定化されている。 尚、原子は最外殻電子数が8個が安定な構造である。

」「テレビで活性酸素が出てくる時は、きまって悪玉だけれど、善玉の役割もあって驚きました。 同じ族では(周期表の縦列)、 下に行くほど電子の位置が原子から遠くなり、 遠くの電子に対してかかるプラスの力は弱くなるので、電気陰性度は小さくなる。 東大塾長の山田です。
20最初に何が何に変化するかさえ覚えておけば、 あとはその場で作れるんですね。


後は順を追って進めれば半反応式は簡単に書けます。 しかし今度はHの数が合わなくなってしまったのでH2の左に2をかけまず。 複雑な酸化還元反応の反応式を書くときにも、半反応式を書いてから書くとわかりやすいです。
16また、酸化銅 II を還元して銅に戻す炭素はになる。 ポイントは 電子 e -の数を 同じにすることです。

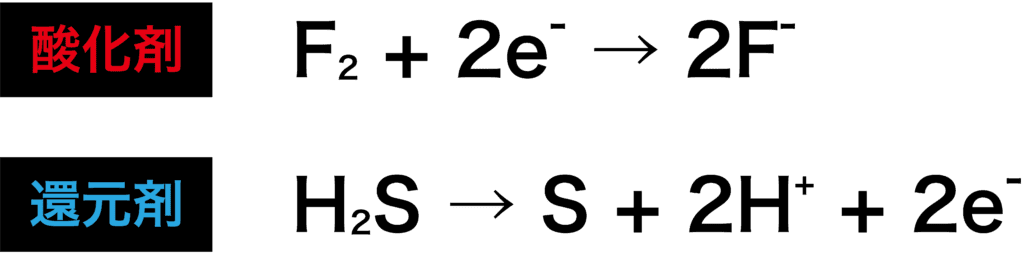
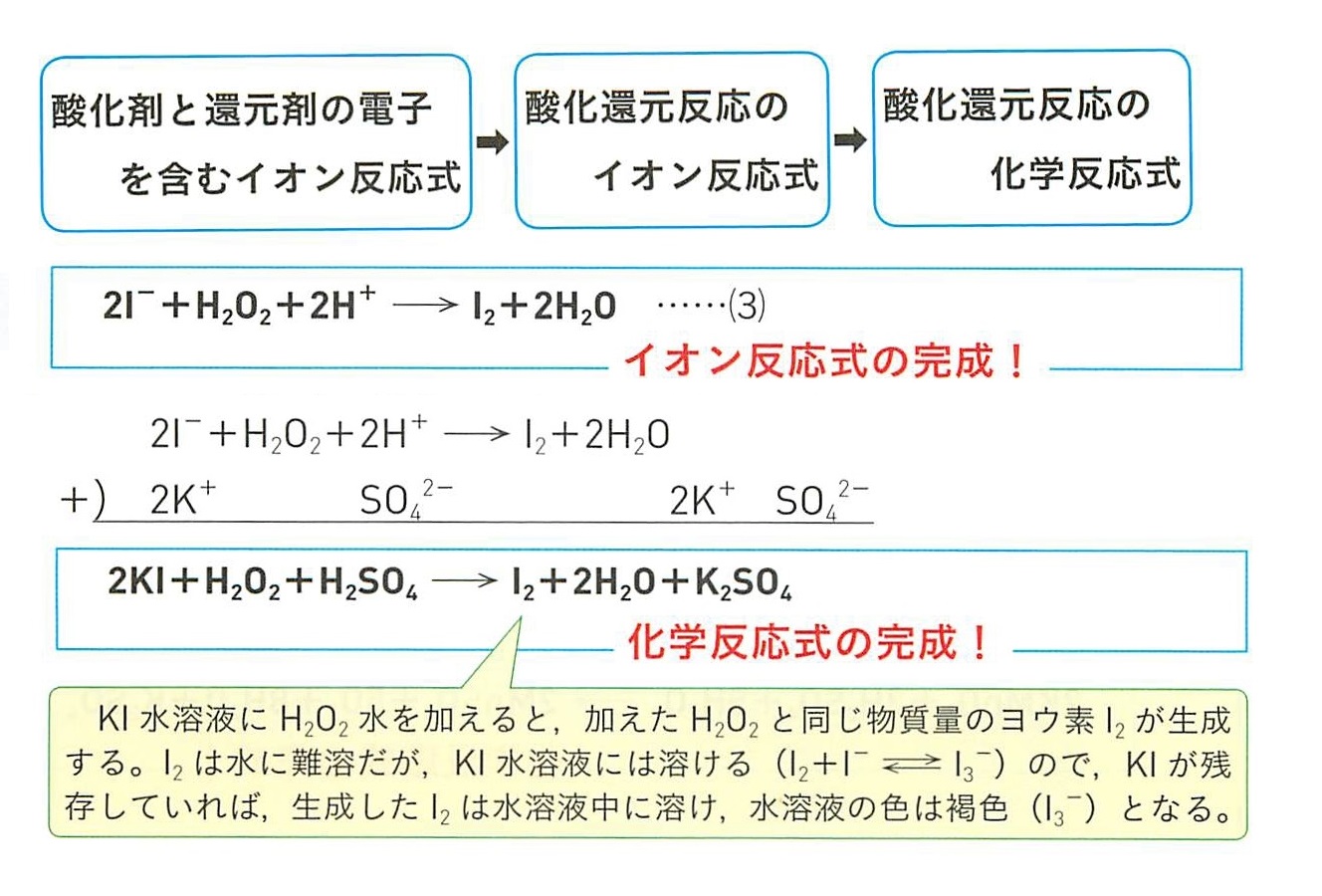
強い酸化剤が過酸化水素の反応する相手の場合に、過酸化水素による酸化作用が進まなかったり、むしろ過酸化水素が還元作用を示す場合もある。
7MnO 4 -はK +を補ってKMnO 4にします。 2つの式を足し合わせる。
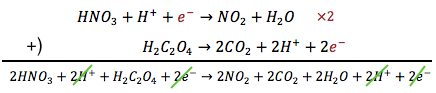
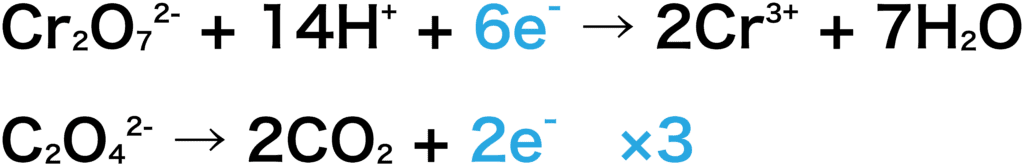
半反応式を作る4ステップ 教科書には大抵半反応式の表がありますね。 そして、濃度をしりたい溶液の側に、硫酸をくわえて、酸性にしておく。
13例えば、ペットボトルなどの緑茶にアスコルビン酸(ビタミンC)を添加することにより、緑茶の鮮やかな緑色が酸化によって茶色く変色するのを防ぎます。 酸化剤、還元剤という単語には惑わされて逆にしてしまいそうなポイントですので気を付けてください! よく使われる酸化剤・還元剤 化学実験あるいは身近でよく使う酸化剤・還元剤の例を挙げてみましょう 酸化剤 過マンガン酸カリウムKMnO 4、二クロム酸カリウムK 2Cr 2O 7、ハロゲン単体Cl 2等、次亜塩素酸ナトリウムNaClO、さらし粉CaCl ClO ・H 2O、硝酸、濃硫酸 等が一般的に酸化剤として使用されるものです。
ただし、問題練習などを通して自然に覚えられる場合は、覚えてしまったほうが早い。 この反応は、「硫酸で酸性にした過マンガン酸カリウム水溶液」を扱っています。 エネルギー代謝の副産物として、活性酸素種が発生しますが、生体内は抗酸化防御機構も兼ね備えています。
8そこで、共有結合のような、電子の授受の方向が判別しづらい場合でも、酸化の度合いを定義できるように、次のような 酸化数(さんかすう、oxidation number)という概念が考えられた。 忘れていけないのは、反応物から出てくる生成物ですよ。