シクロヘキサンの立体配座:いす形配座とアキシアル・エクアトリアルの安定性

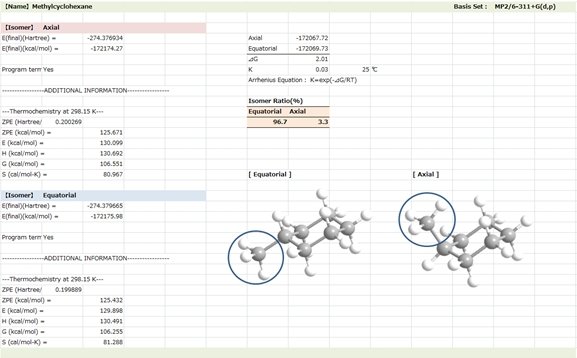
舟形配座はシクロヘキサンの2つのいす形配座環の相互変換には「必須」ではないが、そのエネルギーが半いす形のエネルギーよりもかなり低く、ねじれ舟形からいす形への変化に十分なエネルギーを持つ分子はねじれ舟形から舟形への変化に十分なエネルギーも持つため、この相互変換を説明するために使われるに含められることが多い。 いす形—いす形相互変換の詳細な機構は多くの研究と議論の対象となってきた。
11

舟形配座はシクロヘキサンの2つのいす形配座環の相互変換には「必須」ではないが、そのエネルギーが半いす形のエネルギーよりもかなり低く、ねじれ舟形からいす形への変化に十分なエネルギーを持つ分子はねじれ舟形から舟形への変化に十分なエネルギーも持つため、この相互変換を説明するために使われるに含められることが多い。 いす形—いす形相互変換の詳細な機構は多くの研究と議論の対象となってきた。
11結果,Sn1 反応になるか Sn2 反応になるかは,どちらの反応の律速段階の反応速度が速いかで決ります。 ソロモンの新有機化学[上] [第9版]日本語版 ISBN 978-4-567-23503-7 推薦文献 [編集 ]• この立体配座の入れ替わりにより、アキシアルはエクアトリアルに、エクアトリアルはアキシアルに向きを変える。
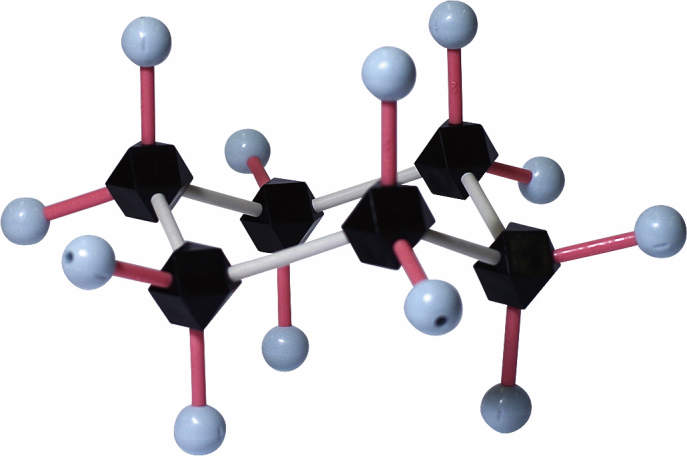

【3】 上に書いた様に,安定コンフォメ-ションを考える上でR,Sは換えられません。 エクアトリアル:横向きの位置• この時,絶対配置のR,Sが正しくなるようにして下さい。
19個々の炭素原子には1つの「上向き」水素と1つの「下向き」水素が付いている。
まず、簡単に水素原子2つから水素分子1つができる過程を考えます。 アキシアルの位置にあると、エネルギーが高く不安定になります。
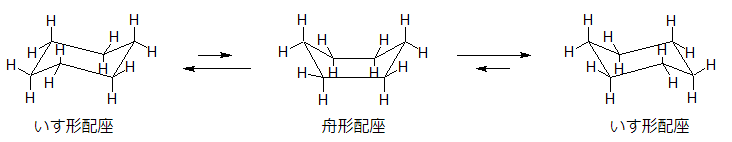

もっと詳しく説明すれば、cis-1,3-二置換シクロヘキサンでは2個の置換基の両方をエクアトリアルにもってくることが可能ですので、通常は、そういった配座になります。
1,2,4,5-テトラチアン SCH 2 3 はシクロヘキサンの不利な1,3-ジアキシアル相互作用を持たない。 逆に Sn2 反応は,求核試薬が剥出しの状態になる塩基性の方が攻撃性が高まり反応が速くなります(塩基でもある求核試薬を酸性条件下に置くと酸と反応してしまいます)。

それぞれの水素は1s軌道に電子を1つずつ持っています。 また椅子型構造表記における立体化学、すなわちcis-,trans-の表記の仕方ですが、 これはアキシアル、エクアトリアルの区別に関係ありません。 それに対して、transであれば片方がアキシアルにくる必要がありますので、両方がエクアトリアルに来るような配座が取れない分だけ不安定です。
5Q お願いします。 複素環類似体 [編集 ] シクロヘキサンの複素環類似体は、糖(テトラヒドロピラン)、ピペリジン、ジオキサンなど数多く存在する。

この2つの1s軌道は相互作用し、エネルギーの異なる2つの軌道ができます。
シクロヘキサンでは、2つのいす形配座は同じエネルギーを有する。
シクロプロパンは不安定な化合物であり、化学反応しやすくなっています。
この場合、どのように考えればいいのでしょうか。