イオン化 傾向 覚え 方 下 ネタ

ひどすぎる借金。 スポンサーリンク 化学の勉強法 カテゴリ一覧• 例えば 問 薄い塩酸に亜鉛と銅の金属板を入れて電池を作ります。 はへのなりやすさを表した序列です。
20

ひどすぎる借金。 スポンサーリンク 化学の勉強法 カテゴリ一覧• 例えば 問 薄い塩酸に亜鉛と銅の金属板を入れて電池を作ります。 はへのなりやすさを表した序列です。
20反対に、みんなと遊んでいても、気づくといつのまにか一人になってしまうタイプの人もいますが、この人は 『イオン化傾向が小さく』 『還元しやすい』人だということになります。
[…]• 化学電池のしくみ 化学変化を利用して、化学エネルギーを電気エネルギーに変換する装置を 「 化学電池」といいます。 はZn>H、の方がイオンになりやすいのに がイオンじゃなくて、水素がイオンの状態でいるなんて変ですよね。

になりやすい、それはつまり、電子を放出しやすい(=電子が原子から外れやすい)ということを意味します。 基本は、これで終了です。
ここでは、単純に 『酸の三兄弟(塩酸・硫酸・硝酸)』の酸化力の強さを示しておきます。 こちらも金属元素の反応を理解する上で重要になるものなので、しっかりと目を通しておきましょう! ところで下の問題は、今年度 H29年度 の大学入試センター試験 追試験 「化学基礎」で出題されたものです。
たとえば、とを使うでは、亜鉛が負極になり、銅が正極になる(電解液はの果汁である)。
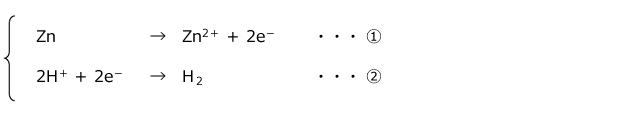

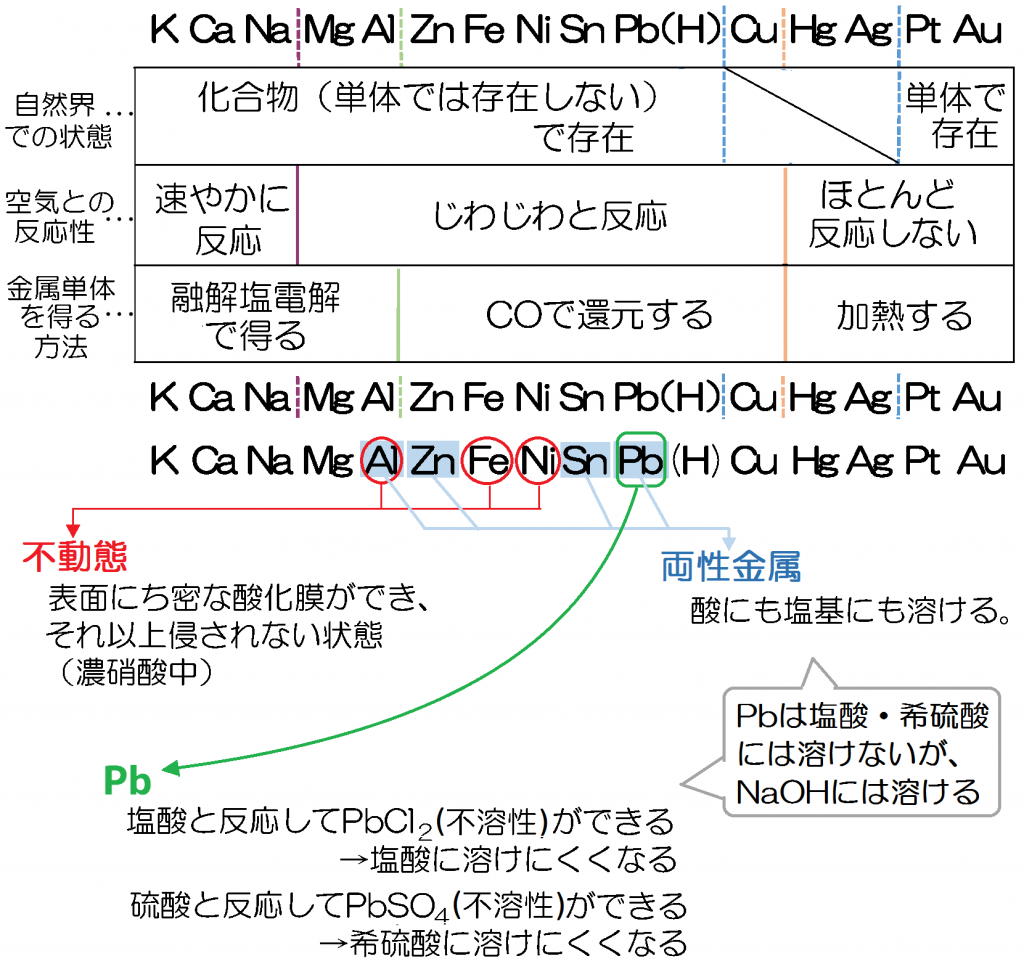
高校生になってから覚えても遅くないですよ。 単体を作るためには化合物中の金属イオンを還元する必要があります。 になりやすい順に金属を並べたものがでした。
は電池の分野でも使う大切な原理となっていますので、ここでしっかりマスターしましょう。 (黄銅)」 振られた博多の中坊さんからの投稿 白銅(Cu+Ni) どうにか吐くど~ クラークさんからの投稿 黄銅、青銅、白銅 明(Zn)日 Sn に Ni はこうせい吐く いちぢさんからの投稿 信号の色 進め Sn 青 青銅 あえて Zn 黄色 黄銅 で止まるのは ニッコリ Ni 白バイ 白銅 後ろから まりりさんからの投稿 ステンレス(Fe+Cr+Ni) ステンレスのテクニック クラークさんからの投稿 徹 Fe 夜して苦労 Cr 人 Ni が作ったステンレス ふぇぶるさんからの投稿 ジュラルミン(アルミニウムと銅・マグネシウムなどの合金) 「ジュラルミンある(Al)よ。


単体の製法 最後に金属の単体の製法も確認しておきましょう。 イオン化エネルギーは、電子を1個取り去るのに必要なエネルギーですよね。 2019. しかし、酸化還元反応の進む方向は単にイオン化エネルギーの大小だけではなく、イオンの溶液中での安定性や電気化学活量などとして反応が進む方向を決定づける他の因子に大きく影響される。
先程言葉足らずで申し訳ないですが、イオン化傾向は水溶液中と定義されているので、主様のおっしゃる通り水和している状態を経ます。

そして、電子の外れやすさというのは基本的に 同族元素なら、が大きいほど(で下に行くほど)電子は外れやすい です。 また、水溶液中でイオン化エネルギーによってイオン化することは理論的に可能です。 ただし、意味は分かるようにしておきましょう。
11実際に書いてみると、 みたいな感じです。
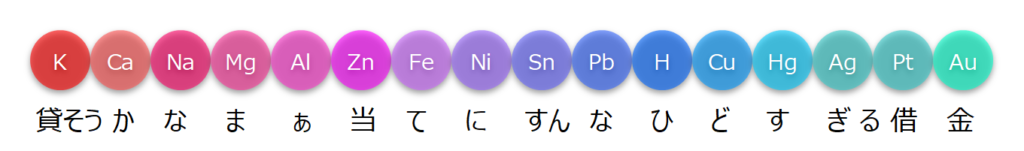
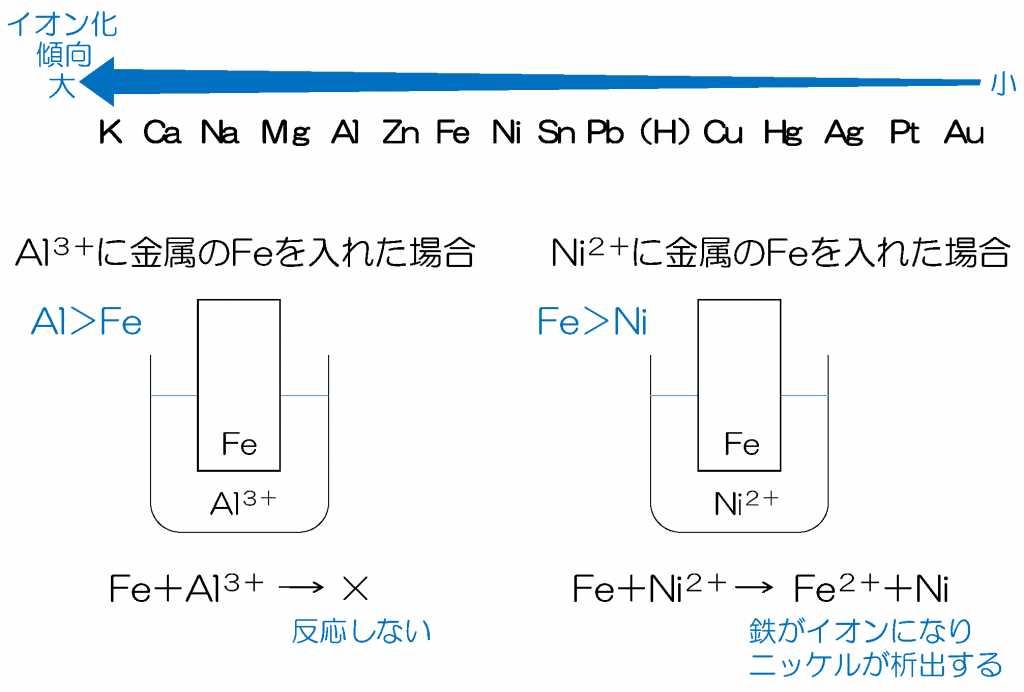
原子は種類によってイオンになりやすさが違うのです。 教科書的な説明はしないと言いましたが、ただ、覚えやすさにも関係してくるので、一応 イオン化列の意味することを書いておきます。 まあ、あてにすんな。
ですから中3理科でよく出る原子について覚えていきましょう。 しかし正確には、前述の説明のようにイオン化の容易さではなく、二つの元素のどちらがより酸化され易い(あるいは還元され易い)か、つまり酸化還元反応における化学平衡がどちらに偏っているかの序列である。
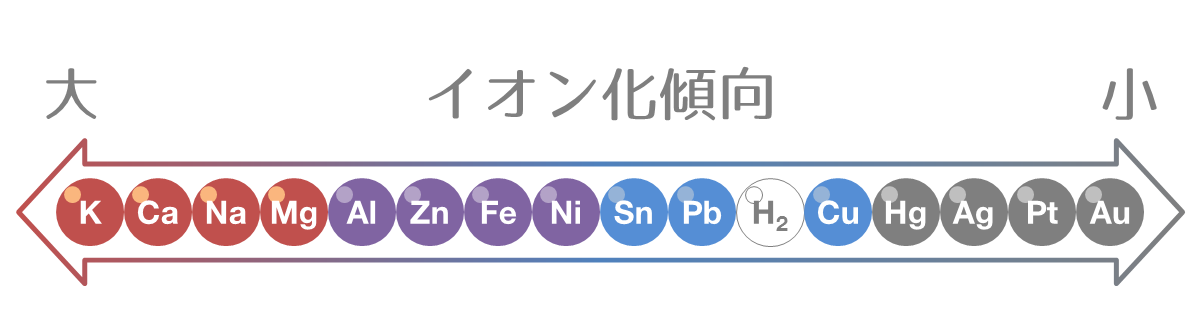
イオン化傾向とは?図を使って丁寧に解説! まずはイオン化傾向がそもそもなんなのかを考えましょう。 これは電池へと繋がる大切な部分ですので、しっかりと覚えておいてください。 つまり、 でいうと、左下に行けば行くほど、電子が外れやすい。
7イオン化傾向では、次の金属を覚えます。 ブログでは伝えきれない、 勉強の成果をきっちりと挙げる方法や、 受験勉強の考え方などをお伝えしようと思っています。