有機反応機構(カルボニル基に対する求核付加反応)
-oside+グリコシド.jpg)

ASかPCを考えておりますが、 ASはPCより耐衝撃性が低く、検討している製品の形状には強度が足りないと思っております。
12医療人にふさわしい質の高さを備え、患者さんから信頼される薬剤師を養成• すると、例えば 1 では光が右に15度、 2 では左に15度回転してしまいます。 逆にpHを上げていくとCOOHはCOO-になり、NH2. ここで,両原子の 1s 軌道の電子は結合には関与しませんので考えなくても良いです。
大容量のバイアルをボトルと呼ぶことがありますが、これは慣用的な呼び名で、厳密にどの大きさからと決まっているわけではありません。

安定性に寄与する主要な要因は、 (安定化) 電子求引性基(通常酸素あるいは原子)が環の配置にあるアノマーを安定化させる。 ご質問の上のフィッシャー投影式ですと、上の 1 を適用して、「COOHを上に移動、CH3を下に移動、Hを右に移動」という形で循環的に入れ替えると、左にアミノ基が来てL型であることがわかります。
また、原核生物ではひとつのmRNAが複数の関連のあるタンパク質を同時にコードしているポリシストロン性が見られますが、真核生物では通常ひとつのmRNAからは一種類のタンパク質しかできません(モノシストロン性)。 遷移元素化学において混成理論を用いることは可能ですが、上で述べたように一般的に正確ではないのです。
その結果のベクトルが0になれば,部分的には電気双極子モ-メント(極性)が存在しても,分子全体としては電気双極子モ-メント(極性)が存在しない事(つまり,非極性)になります。
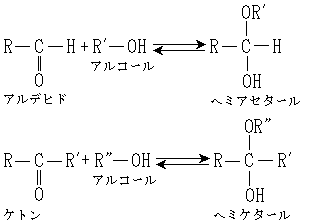
しかし、ヘミアセタール以外のOHだった場合、このように埋めてくれる『 Oの非共有電子対』のような存在がありません。
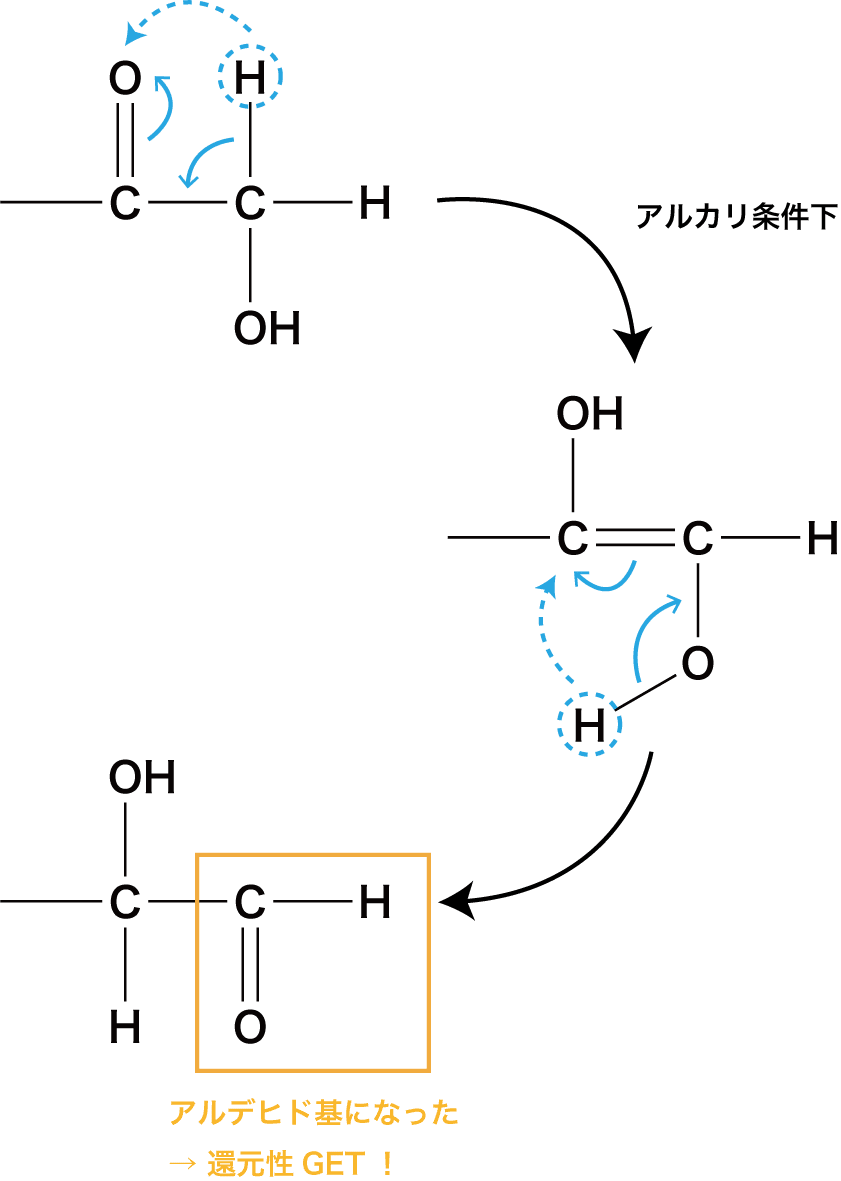
各々の殻の最大数の計算方法は決まっており2n 2と表せれるのです。 すなわち、カルボニル基 - CO - に対する求核付加反応には、「酸性条件下でルイス酸であるカルボニル化合物を強くする方法」と、「塩基性条件下で強力な求核剤を用いる方法」の 2 つがあるのです。
一方、最外殻電子軌道以外の内殻軌道 内側の軌道 が閉殻の金属である3つの亜鉛族元素のグループである亜鉛 Zn やカドミウム Cd や水銀 Hg は、電子配置も化学的性質も典型元素の金属に近いので遷移元素とはされません。
この反応は、工業的にも銀メッキの手法として利用されており、アルデヒドとしては、安価なホルムアルデヒド HCHO が使用されます を参照。 まず「水溶液中での平衡」ですけど、 ヘミアセタール基がないので平衡状態は特にありませんよね? で、開かないためにアルデヒド基が出てこないから還元性がないんですよね? 次に「単糖同士の結合」なんですが、これは何なのでしょうか? (そもそも、グリコシド結合というのが何なのかよくわかんないんですが・・・) いつも質問が多くて申し訳ありません。
』との事から,勝手に「炭素・窒素間の結合」についての「初歩的レベルの話」と考えましたが・・・。 ヘミアセタールとアセタールは実質的に、電気的に中性な四面体型中間体である。

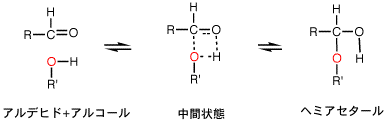
電子軌道は内側から1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、5p…というように原子番号が大きくなればなるほど、電子軌道も増えていきます。 また、この製法ではあまり大容量のものはつくれません。 また、酸素原子には、結合に関与していない非共有電子対が 2 組存在し、その軌道は、カルボニル炭素とそれに結合した原子 3 個が作る平面と同一平面に存在しています。
20そのためヘミアセタールは還元性がある。 また同一原子の個数を示すために元素記号の右下付き添え字をつけて表現します。